Ideal gaz holati tenglamasi
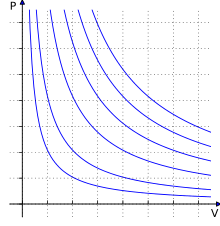
Umumiy gaz tenglamasi deb ham ataladigan ideal gaz qonuni gipotetik ideal gazning holat tenglamasidir. Bu bir nechta cheklovlarga ega boʻlsa-da, koʻp sharoitlarda koʻplab gazlarning xatti-harakatlarining yaxshi yaqinlashuvidir. Bu birinchi marta 1834-yilda Benoit Pol Emile Klapeyron tomonidan empirik Boyl qonuni, Charlz qonuni, Avogadro qonuni va Gey-Lyusak qonunining kombinatsiyasi sifatida taʼkidlangan. Ideal gaz qonuni koʻpincha empirik shaklda yoziladi:bu yerda
p- bosim,
V-hajm
T-harorat ;
– ideal gaz doimiysi hisoblanadi.
U 1856-yilda Avgust Krönig [1] va 1857-yilda Rudolf Klauzius [2] erishgan (aftidan mustaqil ravishda) mikroskopik kinetik nazariyadan ham olinishi mumkin.
Formulalari
[tahrir | manbasini tahrirlash]
Gaz miqdorining holati uning bosimi, hajmi va harorati bilan belgilanadi. Tenglamaning zamonaviy shakli ularni ikkita asosiy shaklda bogʻlaydi. Holat tenglamasida ishlatiladigan harorat mutlaq haroratdir: tegishli SI birligi kelvindir.
Umumiy shakllar
[tahrir | manbasini tahrirlash]Eng koʻp kiritilgan shakllar:bu yerda:
- – gazning mutlaq bosimi ,
- – gazning hajmi ,
- – gaz moddasining miqdori (mol soni deb ham ataladi),
- – Boltsman doimiysi va Avogadro doimiysi mahsulotiga teng ideal yoki universal gaz doimiysi ,
- – Boltsman doimiysi ,
- - Avogadro doimiysi ,
- – gazning mutlaq harorati ,
- – gazning zarrachalari (odatda atomlar yoki molekulalar) soni.
SI birliklarida p paskalda, V kub metrda, n molda va T kelvinda oʻlchanadi (Kelvin shkalasi Selsiy boʻyicha siljish shkalasi boʻlib, bu yerda 0,00 K = −273,15 °C, mumkin boʻlgan eng past harorat).). R qiymati 8,314 J/(mol·K) = 1,989 ≈ 2 kal/(mol·K) yoki 0,0821 L⋅atm/(mol⋅K) qiymatiga ega.
Molar shakli
[tahrir | manbasini tahrirlash]Qancha gaz borligini gazning kimyoviy miqdori oʻrniga massasini berish orqali aniqlash mumkin. Shuning uchun ideal gaz qonunining muqobil shakli foydali boʻlishi mumkin. Kimyoviy miqdori, n (molda) gazning umumiy massasiga (m) (kilogramm) molyar massaga, M (mol uchun kilogramm) boʻlinganiga teng:
n ni m / M bilan almashtirib, keyinchalik r = m / V zichligini kiritib, biz quyidagilarni olamiz:
Oʻziga xos gaz konstantasini R spesifik (r) R / M nisbati sifatida belgilash,
Ideal gaz qonunining bu shakli juda foydalidir, chunki u bosim, zichlik va haroratni koʻrib chiqilayotgan gaz miqdoridan mustaqil formulada bogʻlaydi. Shu bilan bir qatorda, qonun oʻziga xos hajm v boʻyicha, zichlikning oʻzaro nisbati sifatida yozilishi mumkin.
Ayniqsa, muhandislik va meteorologik dasturlarda oʻziga xos gaz konstantasini R belgisi bilan ifodalash keng tarqalgan. Bunday hollarda universal gaz konstantasi odatda boshqa belgi bilan beriladi, masalan yoki uni farqlash uchun. Har qanday holatda, gaz konstantasining konteksti va/yoki birliklari universal yoki maxsus gaz konstantasi ishlatilayotganligini aniq koʻrsatishi kerak. [3]
Statistik mexanika
[tahrir | manbasini tahrirlash]Statistik mexanikada quyidagi molekulyar tenglama birinchi tamoyillardan kelib chiqadi :
Bu yerda P – gazning mutlaq bosimi, n – molekulalarning soni zichligi (n = N/V nisbati bilan berilgan, oldingi formuladan farqli oʻlaroq, n – mollar soni), T – mutlaq harorat, va kB – harorat va energiyaga bogʻliq boʻlgan Boltsman doimiysi, quyidagicha ifodalanadi:
Bu yerda NA – Avogadro doimiysi .
Bundan koʻramizki, massasi m boʻlgan, oʻrtacha zarracha massasi atom massasi konstantasi μ ga teng boʻlgan gaz uchun mu, (yaʼni, massa μ u) molekulalar soni quyidagicha boʻladi.
va ρ = m/V = nμmu boʻlgani uchun ideal gaz qonunini quyidagicha qayta yozish mumkinligini topamiz.
Kombinatsiyalangan gaz qonuni
[tahrir | manbasini tahrirlash]Charlz, Boyl va Gey-Lyussak qonunlarini birlashtirib, birlashgan gaz qonunini beradi, u ideal gaz qonunida aytilgan mollar soni aniqlanmagan va nisbati bir xil funktsional shaklni oladi. uchun oddiygina doimiy sifatida qabul qilinadi: [4]
bu yerda gaz bosimi, gazning hajmi, gazning mutlaq harorati, va doimiy hisoblanadi. Xuddi shu moddani ikki xil shartlar toʻplamida taqqoslaganda, qonun quyidagicha yozilishi mumkin
- Boyl qonuni (Equation 1)
- Charlz qonuni (Equation 2)
- Avogadro qonuni (Equation 3)
- Gey-Lyussak qonuni (Equation 4)
- Equation 5
- Equation 6
Shuningdek qarang
[tahrir | manbasini tahrirlash]- Boltsman doimiysi – Zarrachalar kinetik energiyasini harorat bilan bogʻlovchi fizik konstanta Konfiguratsiya integrali – Termodinamika va statistik fizikadagi funksiya Dinamik bosim – suyuqlik hajmining birligi uchun kinetik energiya Gaz qonunlari Ichki energiya – Tizimdagi energiya Van der Waals tenglamasi – Gazning ideal boʻlmagan harakatini hisobga oladigan gaz holati tenglamasi
Maʼlumotnomalar
[tahrir | manbasini tahrirlash]- ↑ Krönig, A. (1856). "Grundzüge einer Theorie der Gase" (de). Annalen der Physik und Chemie 99 (10): 315–22. doi:10.1002/andp.18561751008. https://zenodo.org/record/1423642. Facsimile at the Bibliothèque nationale de France (pp. 315–22).
- ↑ Clausius, R. (1857). "Ueber die Art der Bewegung, welche wir Wärme nennen" (de). Annalen der Physik und Chemie 176 (3): 353–79. doi:10.1002/andp.18571760302. https://zenodo.org/record/1423644. Facsimile at the Bibliothèque nationale de France (pp. 353–79).
- ↑ Moran. Fundamentals of Engineering Thermodynamics, 4th, Wiley, 2000. ISBN 0-471-31713-6.
- ↑ Raymond, Kenneth W.. General, organic, and biological chemistry : an integrated approach, 3rd, John Wiley & Sons, 2010 — 186-bet. ISBN 9780470504765. Qaraldi: 2019-yil 29-yanvar.

































