Diazo birikma
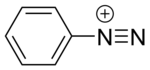
Diazo birikmalar yoki diazo tuzlari umumiy funksional guruhga ega bo'lgan organik birikmalar guruhidir. [R−N+≡N]X− - bu yerda R har qanday organik guruh bo‘lishi mumkin, masalan, alkil yoki aril. X esa noorganik yoki organik anion, masalan, galogendir .
Umumiy xossalari va reaktivligi
[tahrir | manbasini tahrirlash]Arendiazo kationlari va tegishli turlari
[tahrir | manbasini tahrirlash]X-nurli kristallografiyaga ko'ra: C−N+≡N - tipik diazo tuzlarida bog‘lanish chiziqli bo‘ladi. N+≡N benzodiazo tetrafloroboratdagi bog'lanish masofasi 1,083 (3) Å ni tashkil qiladi, [1] dinitrogen molekulasi (N≡N) bilan deyarli bir xil.
Chiziqli erkin energiya konstantalari σm va σp diazo guruhining kuchli elektron tortib olishini ko'rsatadi. Shunday qilib, diazo bilan almashtirilgan fenollar va benzoik kislotalar o'zlarining almashtirilmagan analoglari bilan solishtirganda pK a qiymatlarini sezilarli darajada kamaytiradilar. 4-gidroksibenzodiazoniyning fenol protonining pK a si fenolning o'zi uchun 9,9 ga nisbatan 3,4 [2] ga teng. Boshqacha qilib aytganda, diazo guruhi pK a ni (kislotalikni oshiradi) million barobarga kamaytiradi.
Arenediazon tuzlarining barqarorligi qarshi ionga juda sezgir. Fenildiazo xlorid xavfli portlovchi hisoblanadi, ammo benzodiazo tetrafloroborat skameykada oson ishlov beriladi.
SN1 va SN2 reaksiyalari yuzaga kelmaydi.
Arendiazo tuzlari keyingi bo'limlarda tavsiflanganidek ko'p qirrali reagentlardir. [3] Elektrofil aromatik almashtirishdan so'ng, diazo kimyosi aromatik birikmalarni tayyorlash uchun eng ko'p ishlatiladigan strategiya hisoblanadi.
Alkanediazo kationlari va tegishli turlar
[tahrir | manbasini tahrirlash]Alkandiazo tuzlari SN2/SN1/E1 almashtirishga nisbatan o'ta reaktivligi tufayli sintetik jihatdan ahamiyatsiz. Biroq, bu kationlar nazariy jihatdan qiziqish uyg'otadi. Bundan tashqari, metildiazo karboksilat diazometan tomonidan karboksilik kislotalarning metillanishida oraliq vosita bo'lib, keng tarqalgan transformatsiya hisoblanadi. [4][5]
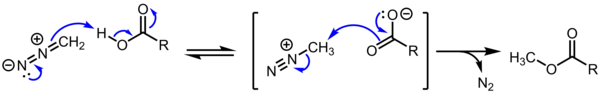
yo'qotish N2 ham entalpik, ham entropik jihatdan qulay:
- [CH3N2]+ → [CH3]+ + N2, ΔH = −43 kcal/mol
- [CH3CH2N2]+ → [CH3CH2]+ + N2, ΔH = −11 kcal/mol
Ikkilamchi va uchlamchi darajali alkandiazo turlari uchun entalpik o'zgarish minimal faollashuv to'sig'i bilan nolga yaqin yoki salbiy deb hisoblanadi. Ikkilamchi va uchlamchi darajali alkandiazo turlari yo bog'lanmagan, mavjud bo'lmagan turlar, yoki eng yaxshi holatda ham juda tez o'tuvchi oraliq mahsulotlardir. [6]
Metandiazoning suvli pKa ([CH3N2]+ ) <10 deb taxmin qilinadi. [7]
Tayyorgarlik
[tahrir | manbasini tahrirlash]Diazo birikmalarni hosil qilish jarayoni "diazotatsiya", "diazonlanish" yoki "diazotizatsiya" deb ataladi. Reaksiya haqida birinchi marta 1858 yilda Piter Griss xabar bergan, u keyinchalik bu yangi birikmalar sinfining bir nechta reaksiyalarini kashf etgan. Ko'pincha diazo tuzlari aromatik aminlarni nitrit kislotasi va qo'shimcha kislota bilan reaksiya orqali tayyorlanadi. Odatda nitrit kislotasi natriy nitrit va ortiqcha mineral kislotadan (odatda suvli HCl,H2SO4, p-H3CC6H4SO3H, yoki H[BF4] ):
- ArNH2 + HNO2 + HX → [ArN2]+X− + 2 H2O

An'anaviy ravishda anilin, natriy nitrit va xlorid kislotadan tayyorlangan diazo kationining xlorid tuzlari xona haroratida beqaror va klassik ravishda 0-5 °C haroratda tayyorlanadi. Shu bilan birga, diazo birikmalarini tetrafloroborat yoki tosilat tuzlari [8] sifatida ajratib olish mumkin, ular xona haroratida barqaror qattiq moddalardir. [9] Ko'pincha diazo tuzining eritmada qolishi ma'qul, lekin ular o'ta to'yingan bo'ladi. [10]
Ushbu xavflar tufayli diazo birikmalari ko'pincha izolyatsiya qilinmaydi. Buning o'rniga ular in situ ishlatiladi. Bu yondashuv arensulfonil birikmasini tayyorlashda ko'rsatib o'tilgan: [11]
Diazo-birikma reaksiyalari
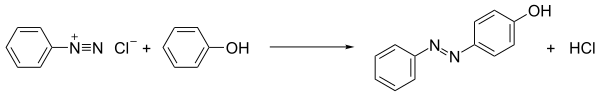
[tahrir | manbasini tahrirlash]Diazo tuzlarining birinchi qoʻllanishi matoni diazoniy birikmasining suvli eritmasiga kiritish, soʻngra bogʻlovchi eritmasiga (elektrofil oʻrinbosar boʻlgan elektronga boy halqa) kiritish orqali suvga chidamli boʻyalgan matolarni ishlab chiqarish edi. Diazo birikmalarining asosiy qo'llanilishi bo'yoq va pigment sanoatiga to'g'ri keladi.
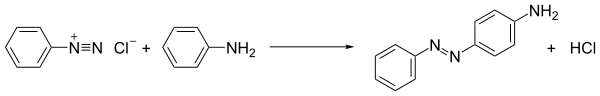
Diazo tuzlarining eng ko'p qo'llaniladigan reaksiyasi azo bo'yoqlar ishlab chiqarishda ishlatiladigan azo birlashma bo'lib qolmoqda. [12] Bu jarayonda diazo birikmasiga elektronga boy substratlar qo'shiladi. Birlashtiruvchi sheriklar anilinlar va fenollar kabi arenlar bo'lsa, jarayon elektrofil aromatik almashtirishga namuna bo'ladi:
- [ArN2]+ + Ar'H → ArN2Ar' + H+
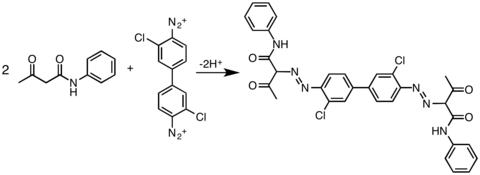
Tijoriy jihatdan kerakli bo'lgan boshqa bog'lovchi sheriklar sinfi asetoasetik amidlar bo'lib, ular diarilid pigmenti sariq pigment 12 ni tayyorlashda ko'rsatilgan.
Olingan azo birikmalar ko'pincha foydali bo'yoqlar bo'lib, aslida azo bo'yoqlar deb ataladi. Masalan, anilin sariq deb ataladigan bo'yoq anilin va diazo tuzining sovuq eritmasini aralashtirib, keyin uni kuchli silkitish orqali hosil bo'ladi. [13] Xuddi shunday, Naftalin-2-ol (beta-naftol) ning sovuq asosli eritmasi kuchli to'q sariq-qizil cho'kma beradi. [13] Metil apelsin laboratoriyada pH ko'rsatkichi sifatida ishlatiladigan azo bo'yoqning namunasi hisoblanadi.
N2 guruhning siljishi
[tahrir | manbasini tahrirlash]Arenediazo kationlari bir qancha reaksiyalarga kirishadi. N2 guruhi boshqa guruh yoki ion bilan almashtiriladi. Asosiylaridan ba'zilari quyidagilardir: [14][15]
Biaril birikmasi
[tahrir | manbasini tahrirlash]Bir juft diazo kationlari biaril hosil qilish uchun birlashtirilishi mumkin. Ushbu konversiya antranilik kislotadan olingan diazo tuzining difenik kislota hosil qilish uchun ulanishi bilan tasvirlangan ((C6H4CO2H)2). [16] Tegishli reaksiyada bir xil diazo tuzi yo'qoladi. N2 va CO2 benzol hosil qiladi. [17]
Galogenidlar bilan almashtirish
[tahrir | manbasini tahrirlash]Sandmeyer reaktsiyasi
[tahrir | manbasini tahrirlash]Benzodiazo xlorid HCl yoki HBr da erigan mis xlorid yoki mis bromid bilan qizdirilsa, mos ravishda xlorbenzol yoki brombenzol hosil bo'ladi.
- [C6H5N2]+ + CuCl → C6H5Cl + N2 + Cu+
Gatterman reaksiyasi
[tahrir | manbasini tahrirlash]Gatterman reaksiyasida benzodiazo xlorid mis kukuni va HCl yoki HBr bilan birgalikda qizdiriladi va mos ravishda xlorbenzol va bromobenzol hosil bo'ladi. Unga nemis kimyogari Lyudvig Gatterman sharafiga nom berilgan. [18]
- 2 Cu + 2 [C6H5N2]+ → 2 Cu+ + (C6H5)2 + 2 N2 (initiation)
- [C6H5N2]+ + HX → C6H5X + N2 + H+ (Cu+ catalysis)
Yodid bilan almashtirish
[tahrir | manbasini tahrirlash]Arendiazo kationlari kaliy yodid bilan reaksiyaga kirishib aril yodid hosil qilishi ma'lum: [19]
- [C6H5N2]+ + KI → C6H5I + K+ + N2
Ftorid bilan almashtirish
[tahrir | manbasini tahrirlash]Ftorbenzol benzodiazoni tetraftorboratning termal parchalanishi natijasida hosil bo'ladi. Ushbu Konversiya Balz-Shieman reaksiyasi deb ataladi. [20]
- [C6H5N2]+[BF4]− → C6H5F + BF3 + N2
An'anaviy Balz-Schiemann reaksiyasi ko'plab motivatsiyalarga sabab bo'ldi, masalan, geksaftorfosfat (V) dan foydalanish ([PF6]−) va geksafluoroantimonat (V) ([SbF6]−) tetraftoroborat o'rniga ([BF4]−). Diazotizatsiya nitrozoniy geksaftoroantimonat (V) kabi nitroziy tuzlari bilan amalga oshirilishi mumkin.[NO]+[SbF6]− . [21]
Turli xil almashtirishlar
[tahrir | manbasini tahrirlash]Vodorod bilan almashtirish
[tahrir | manbasini tahrirlash]Gipofosfat kislotasi, [22] etanol, [23] natriy stanit [24] yoki ishqoriy natriy tiosulfat [25] qaytarilgan arenediazo kationlari benzolni beradi:
- [C6H5N2]+Cl− + H3PO2 + H2O → C6H6 + N2 + H3PO3 + HCl
- [C6H5N2]+Cl− + CH3CH2OH → C6H6 + N2 + CH3CHO + HCl
- [C6H5N2]+Cl− + NaOH + Na2SnO2 → C6H6 + N2 + Na2SnO3 + NaCl
Baeyer va Pfitzinger tomonidan taklif qilingan muqobil usul - diazoguruhni H bilan almashtirish: birinchi navbatda uni gidrazin bilan tasirlashtirish orqali hosil qilish. Keyinchalik mis sulfat eritmasi bilan qaynatish orqali uglevodorodga oksidlanadi. [26]
Gidroksil guruhi bilan almashtirish
[tahrir | manbasini tahrirlash]Fenollar arendiazo tuzlarining suvdagi eritmalarini qizdirish orqali hosil bo'ladi(bunda gidroliz jarayoni sodir bo'ladi): [27][28][29][30]
- [C6H5N2]+ + H2O → C6H5OH + N2 + H+
Bu reaksiya nemischa Phenolverkochung ("fenollar hosil qilish uchun pishirish") deb ataladi. Hosil bo'lgan fenol diazo tuzi bilan reaksiyaga kirishishi mumkin va shuning uchun reaksiya bu keyingi reaksiyani yordam beradigan kislota ishtirokida amalga oshiriladi. [31] Sandmeyer tipidagi gidroksillanishdan foydalanish ham mumkin Cu2O va Cu2+. Ushbu jarayon suvda olib boriladi.
Nitro guruhi bilan almashtirish
[tahrir | manbasini tahrirlash]Nitrobenzolni benzodiazoniy ftorboratni natriy nitrit bilan mis ishtirokida ta'sir ettirish orqali olish mumkin. Shu bilan bir qatorda, anilinning diazotizatsiyasi, o'z-o'zidan mis nitritini hosil qiluvchi mis oksidi ishtirokida amalga oshirilishi mumkin:
- [C6H5N2]+ + CuNO2 → C6H5NO2 + N2 + Cu+
Siano guruhi bilan almashtirish
[tahrir | manbasini tahrirlash]Siano guruhini odatda galoarenlarning nukleofil o'rnini bosishi bilan kiritib bo'lmaydi, ammo bunday birikmalarni diazo tuzlaridan osongina tayyorlash mumkin. Ko'ruvchi sianid reagentidan foydalangan holda benzonitrilni tayyorlash misoli:
- [C6H5N2]+ + CuCN → C6H5CN + Cu+ + N2
Bu reaksiya Sandmeyer reaktsiyasining maxsus turidir.
Triflorometil guruhi bilan almashtirish
[tahrir | manbasini tahrirlash]Ikki tadqiqot guruhi 2013 yilda diazo tuzlarining triftorometilatsiyasi haqida xabar berdi. Goossen tayyorlash haqida ma'lum qildi. CuCF3,CuSCN dan kompleksi,TMSCF3 va Cs2CO3 . Bundan farqli o'laroq, Fu Umemoto reaktivi ( S -triftorometildibenzotiofenium tetraftoroborat) va Cu kukuni (Gattermann tipidagi shartlar) yordamida triftorometilatsiya haqida xabar berdi. Ularni quyidagi tenglama bilan tavsiflash mumkin:
- [C6H5N2]+ + [CuCF3] → C6H5CF3 + [Cu]+ + N2
Qavs misdagi boshqa ligandlar mavjudligini ko'rsatadi, ammo ular kiritilmagan.
Aril guruhi bilan almashtirish
[tahrir | manbasini tahrirlash]Diazo tuzlari ikki bosqichli bajarish tartibida tiollarga aylantirilishi mumkin. Benzendiazo xloridni kaliy etilksantat bilan davolash, so'ngra oraliq ksantat efirini gidrolizlash tiofenolni beradi:
- [C6H5N2]+ + C2H5OCS−2 → C6H5SC(S)OC2H5 + N2
- C6H5SC(S)OC2H5 + H2O → C6H5SH + HOC(S)OC2H5
Boronat efir guruhi bilan almashtirish
[tahrir | manbasini tahrirlash]Aril guruhini arendiazo tuzlari yordamida boshqasiga ulash mumkin. Masalan, benzodiazoniy xloridni benzol (aromatik birikma) bilan natriy gidroksid ishtirokida reaksiyaga kirishi difenilni beradi:
- [C6H5N2]+Cl− + C6H6 → (C6H5)2 + N2 + HCl
Bu reaksiya Gomberg-Bachmann reaksiyasi deb nomlanadi. Xuddi shunday konversiyaga benzodiazo xloridni etanol va mis kukuni bilan ta'sirlashtirish orqali ham erishiladi.
Formil guruhi bilan almashtirish
[tahrir | manbasini tahrirlash]Suzuki-Miyaura oʻzaro bogʻlanish reaksiyalarida qoʻllaniladigan Bpin (pinakolatoboron) guruhini diazo tuzining bi(pinakolato) dibor bilan benzoil peroksid (2) ishtirokida reaksiyasi orqali oʻrnatish mumkin. . [32] Shu bilan bir qatorda shunga o'xshash borillanishga o'tish metalli karbonil komplekslari, shu jumladan dimanganez dekakarbonil yordamida amalga mumkin. [33]
- [C6H5N2]+X− + pinB−Bpin → C6H5Bpin + X−Bpin + N2
Aril diazo tuzini formaldoksim bilan ta'sirlashtirish orqali formil guruhi -CHO ni kiritish mumkin H2C=NOH , so‘ngra aril aldoksim gidrolizlanib, aril aldegid hosil bo‘ladi. [34] Bu reaksiya Beech reaksiyasi deb nomlanadi. [35]
Boshqa dediazotizatsiyalar
[tahrir | manbasini tahrirlash]- elektrodda organik qaytarilish orqali
- askorbin kislotasi ( vitamin C ) kabi yengil qaytaruvchi vositalar [36]
- suvda hosil bo'lgan solvatlangan elektronlardan gamma nurlanishi bilan
- fotoinduktsiyali elektron uzatish
- metall kationlari, ko'pincha mis tuzi bilan qaytarilishi.
- anion induksiyasi: yod kabi qarshi ion aril radikalini va yod radikalini hosil qiluvchi diazoniy kationiga elektron o'tkazishni ta'minlaydi.
Meerwein reaktsiyasi
[tahrir | manbasini tahrirlash]Benzo diazo xlorid faollashtirilgan qo'sh bog'larni ( faollashtiriligan ikki tomonlama aloqa) o'z ichiga olgan birikmalar bilan reaksiyaga kirishib, fenillangan mahsulotlar hosil qiladi. Reaksiya Meerwein arilatsiyasi deb ataladi:
- [C6H5N2]+Cl− + ArCH=CH−COOH → ArCH=CH−C6H5 + N2 + CO2 + HCl
Metall komplekslar
[tahrir | manbasini tahrirlash]Metall komplekslari bilan reaksiyalarida diazo kationlari xuddi shunday harakat qiladi - NO+ . Masalan, quyi valentli metall komplekslari diazo tuzlari bilan birikadi. Tasviriy komplekslar [Fe(CO)2(PPh3)2(N2Ph)]+ va metall-xiral kompleksi Fe(CO)(NO)(PPh3)(N2Ph) . [37]
Payvandlash reaksiyalari
[tahrir | manbasini tahrirlash]Nanotexnologiyada potensial qo'llanilishida diazo tuzlari 4-xlorbenzodiazo tetraftoroborat bir devorli nanotrubalarni juda samarali ishlaydi. [38] Nanotrubalarni tozalash uchun ular ionli suyuqlik bilan ohak va maydalagichda aralashtiriladi. Diazo tuzi kaliy karbonat bilan birga qo'shiladi va aralashmani xona haroratida maydalagandan so'ng nanotrubkalar yuzasi 44 uglerod atomiga 1 samaradorlikda xlorofenil guruhlari bilan qoplanadi. Ushbu qo'shilgan o'rinbosarlar, ular orasidagi katta birlashtiruvchi kuchlar tufayli quvurlarning yaqin to'plamlar hosil bo'lishiga yo'l qo'ymaydi, bu nanotruba texnologiyasida takrorlanadigan muammodir.
Bundan tashqari, aril monoqatlamini tashkil etuvchi diazo tuzlari bilan kremniy qoplamalarini funksionallashtirish mumkin. Bir tadqiqotda kremniy yuzasi ammoniy vodorod ftorid bilan yuvilib, u kremniy-vodorod bog'lari bilan qoplanadi (gidrid passivatsiyasi). [39] Sirtning diazo tuzining asetonitrildagi eritmasi bilan 2 soat davomida qorong'udagi reaksiyasi, erkin radikal mexanizm orqali o'z-o'zidan sodir bo'ladigan jarayon hisoblanadi: [40]

Hozirgacha diazo tuzlarini metallarga payvand qilish quyidagi elementlar yuzalarida amalga oshirilgan: temir, kobalt, nikel, platina, palladiy, rux, mis va oltin. [41] Shuningdek, olmos yuzalariga payvand qilingani haqida ma'lumot mavjud. [42] Qiziqarli savollardan biri sirtdagi aril guruhidagi haqiqiy joylashuvdir. Silikonda o'tkazilgan tadqiqot [43] shuni ko'rsatadiki: titandan misga qadar bo'lgan davrda 4 elementning bog'lanish energiyasi chapdan o'ngga kamayadi, chunki d-elektronlarning soni ortib boradi. Temirning chap tomonidagi metallar yuza tomon egilgan yoki tekis joylashgan bo'lib, metall bilan uglerod pi bog'lari hosil bo'lishiga yordam beradi va temirning o'ng tomonidagilar tik holatda joylashgan bo'lib, metalldan uglerod sigma bog'lanishiga yordam beradi.
Gidrazin guruhiga qisqarish
[tahrir | manbasini tahrirlash]Diazo tuzlarini kaliy xlorid bilan (SnCl2 ) mos keladigan gidrazin hosilalariga kamaytirish mumkin. Bu reaksiya, ayniqsa, triptan birikmalari va indometatsinning Fisher indol sintezida foydalidir. Natriy ditionitdan foydalanish kaliy xloridga nisbatan yaxshiroqdir, chunki u kamroq ekologik muammolarga ega bo'lgan, arzonroq qaytaruvchi moddadir.
Biokimyo
[tahrir | manbasini tahrirlash]Organik kimyoda oz uchraydigan alkandiazo ionlari kanserogenlarning qo'zg'atuvchisi sifatida ishtirok etadi. Xususan, nitrozaminlar alkandiazo turlarini ishlab chiqarish uchun metabolik faollashuvga uchrashi ma'lum.

Xavfsizlik
[tahrir | manbasini tahrirlash]Qattiq diazo galogenidlari ko'pincha xavfli portlovchi hisoblanadi, ular bilan ishlashda o'lim va jarohatlar haqida xabar berilgan. [10]
Anionlarning tabiati tuzning barqarorligiga ta'sir qiladi. Nitrobenzo diazo perxlorat kabi arendiazo perxloratlar portlovchi moddalarni ishga tushirish uchun ishlatilgan.
Yana qarang
[tahrir | manbasini tahrirlash]- Diazo
- Diazo bosib chiqarish jarayoni
- Benzendiazoniy xlorid
- Triazenning parchalanishi
- Dinitrogen kompleksi
Ma'lumotnomalar
[tahrir | manbasini tahrirlash]- ↑ Cygler, Miroslaw; Przybylska, Maria; Elofson, Richard Macleod (1982). "The Crystal Structure of Benzenediazonium Tetrafluoroborate, C6H5N2+•BF4−1". Canadian Journal of Chemistry 60 (22): 2852–2855. doi:10.1139/v82-407. https://archive.org/details/sim_canadian-journal-of-chemistry_1982-11-15_60_22/page/n101.
- ↑ D. Bravo-Díaz, Carlos (2010-10-15), „Diazohydroxides, Diazoethers and Related Species“, in Rappoport, Zvi (muh.), PATai's Chemistry of Functional Groups (inglizcha), John Wiley & Sons, Ltd, doi:10.1002/9780470682531.pat0511, ISBN 9780470682531
- ↑ Norman, R. O. C. (Richard Oswald Chandler). Principles of Organic Synthesis, 3rd, CRC Press, 2017. ISBN 9780203742068. OCLC 1032029494.
- ↑ Streitwieser, Andrew; Schaeffer, William D. (June 1957). "Stereochemistry of the Primary Carbon. VI. The Reaction of Optically Active 1-Aminobutane-1-d with Nitrous Acid. Mechanism of the Amine-Nitrous Acid Reaction1". Journal of the American Chemical Society 79 (11): 2888–2893. doi:10.1021/ja01568a054.
- ↑ Friedman, Lester; Jurewicz, Anthony T.; Bayless, John H. (March 1969). "Influence of solvent on diazoalkane-alkanediazonium ion equilibriums in amine deaminations". Journal of the American Chemical Society 91 (7): 1795–1799. doi:10.1021/ja01035a032.
- ↑ Carey, Francis A.. Advanced organic chemistry, Sundberg, Richard J., 5th, New York: Springer, 2007. ISBN 9780387448978. OCLC 154040953.
- ↑ Fei, Na; Sauter, Basilius; Gillingham, Dennis (2016). "The pK a of Brønsted acids controls their reactivity with diazo compounds" (en). Chemical Communications 52 (47): 7501–7504. doi:10.1039/C6CC03561B. PMID 27212133.
- ↑ Filimonov, Victor D.; Trusova, Marina; Postnikov, Pavel; Krasnokutskaya, Elena A.; Lee, Young Min; Hwang, Ho Yun; Kim, Hyunuk; Chi, Ki-Whan (2008-09-18). "Unusually Stable, Versatile, and Pure Arenediazonium Tosylates: Their Preparation, Structures, and Synthetic Applicability" (EN). Organic Letters 10 (18): 3961–3964. doi:10.1021/ol8013528. ISSN 1523-7060. PMID 18722457.
- ↑ Mihelač, M.; Siljanovska, A.; Košmrlj, J. (2021). "A convenient approach to arenediazonium tosylates". Dyes Pigm. 184: 108726. doi:10.1016/j.dyepig.2020.108726.
- ↑ 10,0 10,1 „UK CRHF Incident Report – Supersaturated Diazonium salt causes Fatality“. UK Chemical Reaction Hazards Forum. 2018-yil 6-oktyabrda asl nusxadan arxivlangan. Qaraldi: 2010-yil 13-may.
- ↑ R. V. Hoffman (1981). "m-Trifluoromethylbenzenesulfonyl Chloride". Org. Synth. 60: 121. doi:10.15227/orgsyn.060.0121.
- ↑ Chemistry of the Diazonium and Diazo Groups: Part 1. S. Patai, Ed. 1978 Wiley-Blackwell. ISBN 0-471-99492-8. Chemistry of the Diazonium and Diazo Groups: Part 2. S. Patai, Ed. 1978 Wiley-Blackwell. ISBN 0-471-99493-6.
- ↑ 13,0 13,1 Clark. „chemguide“. Qaraldi: 2011-yil 28-sentyabr.
- ↑ March, J. “Advanced Organic Chemistry” 4th Ed. J. Wiley and Sons, 1992: New York. ISBN 978-0-471-60180-7.
- ↑ Marye Anne Fox. Organic Chemistry, 3, illustrated, Jones & Bartlett Learning, 2004 — 535–538-bet. ISBN 978-0-7637-2197-8.
- ↑ Atkinson, E. R.; Lawler, H. J. (1927). "Diphenic Acid". Org. Synth. 7: 30. doi:10.15227/orgsyn.007.0030.
- ↑ Logullo, F. M.; Seitz, A. H.; Friedman, L. (1968). "Benzenediazonium-2-carboxy- and Biphenylene". Org. Synth. 48: 12. doi:10.15227/orgsyn.048.0012.
- ↑ L. Gattermann (1894). "Untersuchungen über Diazoverbindungen". Berichte der Deutschen Chemischen Gesellschaft 23 (1): 1218–1228. doi:10.1002/cber.189002301199. http://gallica.bnf.fr/ark:/12148/bpt6k90720c/f1220.chemindefer.
- ↑ Lucas, H. J.; Kennedy, E. R. (1939). "Iodobenzene". Org. Synth. 19: 55. doi:10.15227/orgsyn.019.0055.
- ↑ Flood, D. T. (1933). "Fluorobenzene". Org. Synth. 13: 46. doi:10.15227/orgsyn.013.0046..
- ↑ Furuya, Takeru; Klein, Johannes E. M. N.; Ritter, Tobias (2010). "C–F Bond Formation for the Synthesis of Aryl Fluorides". Synthesis 2010 (11): 1804–1821. doi:10.1055/s-0029-1218742. PMID 20953341. PMC 2953275. //www.pubmedcentral.nih.gov/articlerender.fcgi?tool=pmcentrez&artid=2953275.
- ↑ Reinhard Bruckner, ed. Michael Harmata; Organic Mechanisms Reactions, Stereochemistry and Synthesis 3rd Ed, p.246, ISBN 978-3-8274-1579-0
- ↑ DeTarr, D.F.; Kosuge, T. (1958). "Mechanisms of Diazonium Salt Reactions. VI. The Reactions of Diazonium Salts with Alcohols under Acidic Conditions; Evidence for Hydride Transfer1". Journal of the American Chemical Society 80 (22): 6072–6077. doi:10.1021/ja01555a044.
- ↑ Friedlander, Ber., 1889, 587, 22
- ↑ Grandmougin, Ber., 1907, 40, 858
- ↑ Baeyer & Pfitzinger, Ber., 1885, 18, 90, 786
- ↑ H. E. Ungnade, E. F. Orwoll (1943). "3-Bromo-4-hydroxytoluene". Org. Synth. 23: 11. doi:10.15227/orgsyn.023.0011.
- ↑ Kazem-Rostami, Masoud (2017). "Facile Preparation of Phenol". Synlett 28 (13): 1641–1645. doi:10.1055/s-0036-1588180.
- ↑ Carey, F. A.. Advanced Organic Chemistry. Vol. B, Chapter 11: Springer, 2007 — 1028-bet.
- ↑ Khazaei, Ardeshir; Kazem-Rostami, Masoud; Zare, Abdolkarim; Moosavi-Zare, Ahmad Reza; Sadeghpour, Mahdieh; Afkhami, Abbas (2013). "Synthesis, characterization, and application of a triazene-based polysulfone as a dye adsorbent". Journal of Applied Polymer Science 129 (6): 3439–3446. doi:10.1002/app.39069.
- ↑ R. H. F. Manske (1928). "m-Nitrophenol". Org. Synth. 8: 80. doi:10.15227/orgsyn.008.0080.
- ↑ Wu, Jie; Gao, Yueqiu; Qiu, Guanyinsheng; He, Linman (2014-08-20). "Removal of amino groups from anilines through diazonium salt-based reactions" (en). Organic & Biomolecular Chemistry 12 (36): 6965–6971. doi:10.1039/C4OB01286K. ISSN 1477-0539. PMID 25093920.
- ↑ Fairlamb, Ian; Firth, James D.; Hammarback, L. Anders; Burden, Thomas J.; Eastwood, Jonathan B.; Donald, James R.; Horbaczewskyj, Chris S.; McRobie, Matthew T. et al. (2020). "Light‐ and Manganese‐Initiated Borylation of Aryl Diazonium Salts: Mechanistic Insight on the Ultrafast Time‐Scale Revealed by Time‐Resolved Spectroscopic Analysis". Chemistry – A European Journal 27 (12): 3979–3985. doi:10.1002/chem.202004568. PMID 33135818. https://chemistry-europe.onlinelibrary.wiley.com/doi/10.1002/chem.202004568.
- ↑ „Organic Syntheses Procedure“ (en). 2-bromo-4-methylbenzaldehyde. 2013-yil 20-dekabrda asl nusxadan arxivlangan. Qaraldi: 2021-yil 4-may.
- ↑ Beech, W. F. (1954-01-01). "Preparation of aromatic aldehydes and ketones from diazonium salts" (en). Journal of the Chemical Society (Resumed): 1297–1302. doi:10.1039/JR9540001297. ISSN 0368-1769. https://pubs.rsc.org/en/content/articlelanding/1954/jr/jr9540001297.
- ↑ Pinacho Crisóstomo Fernando (2014). "Ascorbic Acid as an Initiator for the Direct C-H Arylation of (Hetero)arenes with Anilines Nitrosated In Situ". Angewandte Chemie International Edition 53 (8): 2181–2185. doi:10.1002/anie.201309761. PMID 24453180.
- ↑ Sutton, D (1993). "Organometallic Diazo Compounds". Chem. Rev. 93 (3): 905–1022. doi:10.1021/cr00019a008.
- ↑ Price, B. Katherine (2005). "Green Chemical Functionalization of Single-Walled Carbon Nanotubes in Ionic Liquids". Journal of the American Chemical Society 127 (42): 14867–14870. doi:10.1021/ja053998c. PMID 16231941.
- ↑ Michael P. Stewart; Francisco Maya; Dmitry V. Kosynkin et al. (2004). "Direct Covalent Grafting of Conjugated Molecules onto Si, GaAs, and Pd Surfaces from Arenediazonium Salts". J. Am. Chem. Soc. 126 (1): 370–8. doi:10.1021/ja0383120. PMID 14709104.
- ↑ Reaction sequence: silicon surface reaction with ammonium hydrogen fluoride creates hydride layer. An electron is transferred from the silicon surface to the diazonium salt in an open circuit potential reduction leaving a silicon radical cation and a diazonium radical. In the next step a proton and a nitrogen molecule are expelled and the two radical residues recombine creating a surface silicon to carbon bond.
- ↑ Bélanger, Daniel; Pinson, Jean (2011). "Electrografting: a powerful method for surface modification" (en). Chemical Society Reviews 40 (7): 3995–4048. doi:10.1039/c0cs00149j. ISSN 0306-0012. PMID 21503288. http://xlink.rsc.org/?DOI=c0cs00149j.
- ↑ S.Q. Lud; M. Steenackers; P. Bruno et al. (2006). "Chemical Grafting of Biphenyl Self-Assembled Monolayers on Ultrananocrystalline Diamond". J. Am. Chem. Soc. 128 (51): 16884–91. doi:10.1021/ja0657049. PMID 17177439.
- ↑ De-en Jiang; Bobby G. Sumpter; Sheng Dai (2006). "Structure and Bonding between an Aryl Group and Metal Surfaces". J. Am. Chem. Soc. 128 (18): 6030–1. doi:10.1021/ja061439f. PMID 16669660.
- ↑ Tricker, A.R.; Preussmann, R. (1991). "Carcinogenic N-Nitrosamines in the Diet: Occurrence, Formation, Mechanisms and Carcinogenic Potential". Mutation Research/Genetic Toxicology 259 (3–4): 277–289. doi:10.1016/0165-1218(91)90123-4. PMID 2017213.
Havolalar
[tahrir | manbasini tahrirlash]- W. Reusch. „Reactions of Amines“. VirtualText of Organic Chemistry. Michigan State University. 2012-yil 12-dekabrda asl nusxadan arxivlangan.